(Cập nhật quy định phân loại trang thiết bị y tế chẩn đoán in vitro tại Việt Nam)
Trong quá trình đăng ký lưu hành và nhập khẩu trang thiết bị y tế chẩn đoán in vitro (IVD), một trong những bước quan trọng nhất – nhưng cũng dễ sai nhất – chính là phân loại IVD theo Thông tư 05/2022/TT-BYT.
Thực tế triển khai cho thấy, chỉ cần sai một chi tiết nhỏ trong phân loại IVD, doanh nghiệp có thể phải:
- Bị yêu cầu phân loại lại hồ sơ
- Kéo dài thời gian xử lý thêm vài tháng
- Phát sinh chi phí thử nghiệm, bổ sung tài liệu
- Ảnh hưởng đến uy tín pháp lý của sản phẩm
Vì vậy, hiểu đúng và làm đúng ngay từ đầu quy tắc phân loại IVD theo Thông tư 05/2022/TT-BYT là điều vô cùng cần thiết.
Tổng Quan Về Phân Loại IVD Theo Thông Tư 05/2022/TT-BYT
Bài viết này tổng hợp các quy tắc và định nghĩa cốt lõi về việc phân loại trang thiết bị y tế chẩn đoán in vitro (IVD), được ban hành kèm theo Thông tư số 05/2022/TT-BYT của Bộ Y tế. Hệ thống phân loại dựa trên mức độ rủi ro, chia các thiết bị IVD thành bốn loại chính: Loại D (rủi ro cao nhất), Loại C, Loại B, và Loại A (rủi ro thấp nhất). Mức độ rủi ro được xác định chủ yếu dựa trên mục đích sử dụng của thiết bị và tác động tiềm tàng của kết quả xét nghiệm sai đối với sức khỏe cá nhân và cộng đồng.
- Loại D (Rủi ro cao nhất): Bao gồm các xét nghiệm sàng lọc máu, mô, tế bào dùng cho truyền máu hoặc cấy ghép, và các xét nghiệm phát hiện tác nhân lây nhiễm gây bệnh đe dọa tính mạng với nguy cơ lây truyền cao. Một số xét nghiệm xác định nhóm máu và mô quan trọng cũng thuộc loại này.
- Loại C (Rủi ro trung bình-cao): Gồm một loạt các xét nghiệm quan trọng như chẩn đoán bệnh lây qua đường tình dục, xét nghiệm di truyền, sàng lọc trước sinh, theo dõi nồng độ thuốc có nguy cơ cao, và các thiết bị tự xét nghiệm.
- Loại B (Rủi ro trung bình-thấp): Là loại phổ biến, bao gồm tất cả các thiết bị IVD không thuộc các quy tắc phân loại khác. Nhóm này cũng chứa các vật liệu kiểm soát không có giá trị định lượng/định tính.
- Loại A (Rủi ro thấp nhất): Gồm các sản phẩm hỗ trợ, thiết bị dùng chung trong phòng xét nghiệm và vật chứa mẫu.
Các quy tắc phân loại này cung cấp một khuôn khổ pháp lý rõ ràng để quản lý, cấp phép và giám sát các trang thiết bị y tế IVD tại Việt Nam, đảm bảo an toàn và hiệu quả trong chẩn đoán và điều trị.
Các Định Nghĩa Quan Trọng Cần Nắm
Trang thiết bị IVD tự xét nghiệm
Là thiết bị được nhà sản xuất chỉ định cho người không có chuyên môn y tế sử dụng.
Xét nghiệm tại chỗ (Point-of-Care Testing – POCT)
Là xét nghiệm thực hiện ngoài phòng xét nghiệm chuyên nghiệp, như tại giường bệnh hoặc tại nhà.
Tác nhân có thể lây truyền
Là vi sinh vật hoặc yếu tố có khả năng gây bệnh truyền nhiễm cho người.
Sự lây truyền
Là truyền bệnh cho người.
Vật chứa mẫu
Là trang thiết bị IVD chuyên dùng để chứa mẫu bệnh phẩm có nguồn gốc từ cơ thể người.
Thuốc thử
Là các chất hóa học, sinh học, miễn dịch học, các dung dịch hoặc chế phẩm được chủ sở hữu chỉ định sử dụng như trang thiết bị y tế chẩn đoán in vitro.
Chi Tiết 7 Quy Tắc Phân Loại IVD Theo Thông Tư 05/2022/TT-BYT
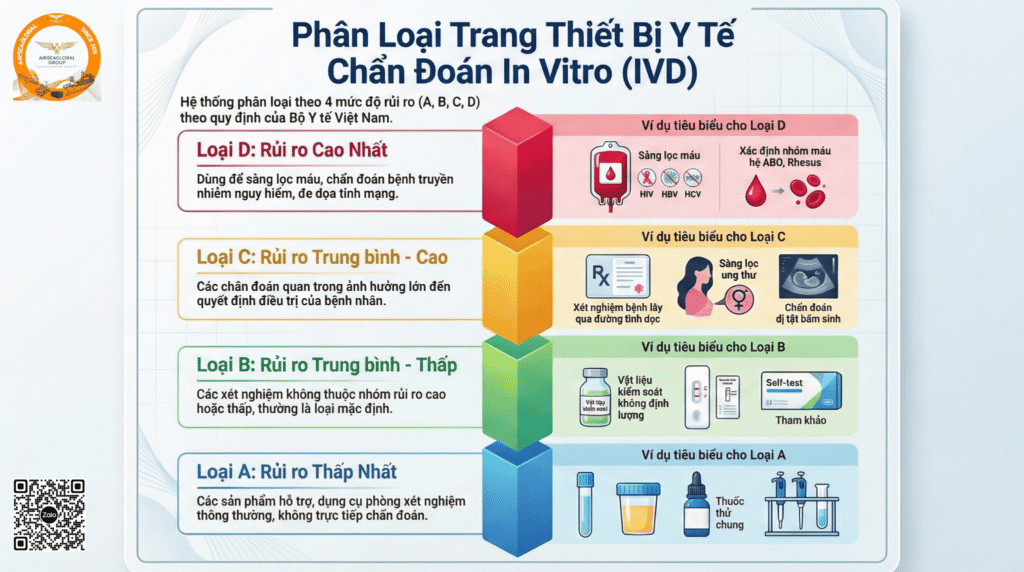
Hệ thống phân loại gồm 7 quy tắc chính, sắp xếp các thiết bị IVD vào 4 loại dựa trên mức độ rủi ro giảm dần từ D đến A.
Quy tắc 1: Trang Thiết Bị Y Tế Loại D (Rủi ro cao nhất)
Một thiết bị IVD được xếp vào Loại D nếu được sử dụng cho một trong hai mục đích sau:
- Sàng lọc trong truyền máu và cấy ghép: Phát hiện sự hiện diện hoặc phơi nhiễm với một tác nhân lây nhiễm trong máu, thành phần máu, mô hoặc bộ phận cơ thể nhằm đánh giá sự phù hợp để truyền hoặc cấy ghép.
- Chẩn đoán bệnh nguy hiểm: Phát hiện sự hiện diện hoặc phơi nhiễm với tác nhân lây nhiễm gây bệnh đe dọa tính mạng, thường không có khả năng chữa trị và có nguy cơ lây truyền cao.
Quy tắc 2: Phân Loại Dựa Trên Xác Định Nhóm Máu và Phân Loại Mô
- Loại C: Các thiết bị IVD dùng để xác định nhóm máu hoặc phân loại mô nhằm đảm bảo tương thích miễn dịch trong truyền máu hoặc cấy ghép.
- Loại D (Ngoại lệ): Các thiết bị dùng để xác định các hệ nhóm máu quan trọng sau đây được xếp vào loại D do mức độ rủi ro cao nếu kết quả sai:
- Hệ ABO: A (ABO1), B (ABO2), AB (ABO3)
- Hệ Rhesus: RH1 (D), Rh2 (C), Rh3 (E), RH4 (c), RH5(e)
- Hệ Kell: Kel1 (K)
- Hệ Kidd: JK1 (Jka), JK2 (Jkb)
- Hệ Duffy: FY1 (Fya), FY2 (Fyb)
Quy tắc 3: Trang Thiết Bị Y Tế Loại C (Rủi ro trung bình-cao)
Một thiết bị IVD được xếp vào Loại C nếu thuộc một trong các trường hợp sau:
- Bệnh lây qua đường tình dục: Phát hiện tác nhân như Chlamydia trachomatis, Neisseria gonorrhoeae.
- Nhiễm trùng máu hoặc dịch não tủy (khả năng lây hạn chế): Phát hiện tác nhân như Neisseria meningitidis hoặc Cryptococcus neoformans.
- Nguy cơ tử vong/khuyết tật nghiêm trọng nếu kết quả sai: Chẩn đoán các bệnh như CMV, Chlamydia pneumoniae, Staphylococcus aureus kháng Methycillin (MRSA).
- Sàng lọc miễn dịch trước sinh: Xác định tình trạng miễn dịch đối với các bệnh như Rubella hoặc Toxoplasmosis.
- Chẩn đoán bệnh nhân có nguy cơ cao: Xác định tình trạng bệnh truyền nhiễm hoặc miễn dịch ở bệnh nhân được cấy ghép (ví dụ: Enterovirus, CMV, HSV) mà kết quả sai có thể dẫn đến quyết định điều trị không phù hợp gây nguy hiểm tính mạng.
- Sàng lọc cho y học cá thể hóa: Lựa chọn bệnh nhân để áp dụng liệu pháp điều trị phù hợp, xác định giai đoạn bệnh hoặc chẩn đoán ung thư.
- Lưu ý: Các thiết bị dùng để theo dõi, hoặc khi quyết định điều trị cần đánh giá sâu hơn, sẽ được xếp vào Loại B theo Quy tắc 6.
- Xét nghiệm gen di truyền ở người: Chẩn đoán các bệnh như Huntington hoặc xơ nang.
- Theo dõi nồng độ thuốc/chất sinh học nguy cơ cao: Theo dõi các chỉ số mà kết quả sai có thể gây nguy hiểm tính mạng tức thời (ví dụ: dấu hiệu tim mạch, cyclosporin, xét nghiệm thời gian đông máu).
- Theo dõi bệnh truyền nhiễm đe dọa tính mạng: Theo dõi tải lượng virus HCV, HIV và xác định kiểu gen.
- Sàng lọc rối loạn bẩm sinh ở thai nhi: Phát hiện các bệnh như tật nứt đốt sống hoặc hội chứng Down.
Quy tắc 4: Thiết Bị Tự Xét Nghiệm và Xét Nghiệm Tại Chỗ
- Trang thiết bị tự xét nghiệm:
- Loại C: Theo quy tắc chung.
- Loại B (Ngoại lệ): Nếu kết quả xét nghiệm không dùng để quyết định điều trị, chỉ có giá trị tham khảo và cần xét nghiệm bổ sung tại phòng xét nghiệm.
- Trang thiết bị xét nghiệm tại chỗ:
- Loại C: Các thiết bị xét nghiệm thông số khí máu và đường huyết.
- Các loại khác: Các thiết bị xét nghiệm tại chỗ khác được phân loại dựa trên các quy tắc tương ứng.
Quy tắc 5: Trang Thiết Bị Y Tế Loại A (Rủi ro thấp nhất)
Các thiết bị IVD được phân vào Loại A nếu thuộc một trong các trường hợp sau:
- Sản phẩm khác tham gia hoặc hỗ trợ quá trình xét nghiệm được chỉ định cho các quy trình chẩn đoán in vitro.
- Trang thiết bị được chủ sở hữu chỉ định sử dụng chung trong các quy trình chẩn đoán in vitro.
- Vật chứa mẫu.
Quy tắc 6: Phân Loại Mặc Định là Loại B (Rủi ro trung bình-thấp)
Những trang thiết bị y tế chẩn đoán in vitro không thuộc phạm vi của các quy tắc từ 1 đến 5 sẽ được phân vào Loại B. Đây là quy tắc bao trùm cho phần lớn các xét nghiệm thông thường.
Quy tắc 7: Vật Liệu Kiểm Soát
Các vật liệu kiểm soát không được gán giá trị định lượng hoặc định tính được phân vào Loại B.
Vì Sao Phân Loại IVD Theo Thông Tư 05/2022/TT-BYT Cực Kỳ Quan Trọng?
Việc phân loại IVD đúng giúp doanh nghiệp:
- ✅ Xác định đúng thủ tục công bố hoặc đăng ký lưu hành
- ✅ Tránh bị yêu cầu bổ sung – phân loại lại – trả hồ sơ
- ✅ Rút ngắn thời gian xử lý
- ✅ Đảm bảo an toàn pháp lý khi nhập khẩu IVD
Những Trường Hợp Doanh Nghiệp Hay Gặp Khó
- Phân vân giữa IVD loại B và C
- Thiết bị tự xét nghiệm nhưng bị đẩy lên loại C
- Sản phẩm đã lưu hành nhưng bị yêu cầu phân loại lại
- Hồ sơ “kẹt” nhiều tháng do mục đích sử dụng mô tả chưa đúng
Lời Kết
Phân loại IVD theo Thông tư 05/2022/TT-BYT không phải là thủ tục hình thức, mà là nền tảng pháp lý cho toàn bộ hồ sơ đăng ký lưu hành và nhập khẩu trang thiết bị y tế chẩn đoán in vitro tại Việt Nam.
Nếu Anh/Chị đang:
- Chuẩn bị nhập khẩu IVD
- Chưa chắc chắn phân loại B hay C
- Từng bị trả hồ sơ vì phân loại chưa phù hợp
👉 Em Minh luôn sẵn sàng trao đổi chi tiết theo từng sản phẩm cụ thể, dựa trên mục đích sử dụng – IFU – hồ sơ kỹ thuật thực tế.
Các bài viết tham khảo liên quan đến thiết bị y tế Chẩn đoán In Vitro (IVD)
MỌI THẮC MẮC VỀ PHÂN LOẠI THIÊT BỊ Y TẾ IN VITRO XIN LIÊN HỆ MS TUYẾT MINH AIRSEAGLOBAL -0971 460 378
Mail: minhntt@airseaglobalgroup.com.vn

CÔNG TY CỔ PHẦN TẬP ĐOÀN AIRSEAGLOBAL
– VUA DỊCH VỤ NHẬP KHẨU THIẾT BỊ Y TẾ –
NHẬN FULL DỊCH VỤ HỖ TRỢ CHECK, CARE, XIN GIẤY PHÉP, VẬN CHUYỂN QUỐC TẾ, THÔNG QUAN, ĐƯA HÀNG VỀ KHO
- Xử lý GIẤY PHÉP chỉ từ 3-5 ngày:
- Phân loại (Chỉ từ 500k - Chuẩn vào thầu)
- Công bố tiêu chuẩn áp dụng đối với TBYT loại A, B
- Đăng ký Lưu hành thiết bị y tế C, D chỉ từ 2 tháng
- Công bố đủ điều kiện mua bán TBYT loại BCD (Chuẩn vào thầu)
- Công bố đủ điều kiện sản xuất, ISO 13485, ISO 9001, CFS
- THÔNG QUAN MỞ TỜ KHAI CHỈ TỪ 800k/tờ khai.
- Vận chuyển quốc tế, trucking nội địa giá SIÊU TỐT, SIÊU NHANH. Bên em thuộc WCA member ID 73213
AIRSEAGLOBAL CUNG CẤP DỊCH VỤ XIN GIẤY PHÉP (CÔNG BỐ A, B; LƯU HÀNH C, D) CHO THIẾT BỊ Y TẾ CHUYÊN NGHIỆP
CAM KẾT HOÀN TIỀN 100% PHÍ DỊCH VỤ NẾU GIẤY PHÉP (CÔNG BỐ, LƯU HÀNH) KHÔNG CHUẨN VÀO THẦU, KHÔNG LẤY ĐƯỢC HÀNG
Airseaglobal Group hiện có hơn 2300 khách hàng thiết bị y tế, thông quan 15,000 tờ khai hải quan hàng y tế, xin giấy phép cho hơn 11.000 loại thiết bị y tế và phụ kiện
Xem full các số đăng ký lưu hành TBYT tiêu biểu Airseaglobal đã làm cho khách hàng (update liên tục) TẠI ĐÂY
Xem full các vận đơn hàng Sea tiêu biểu mà Airseaglobal đã làm cho khách hàng TẠI ĐÂY
Xem full các vận đơn hàng Air tiêu biểu mà Airseaglobal đã làm cho khách hàng TẠI ĐÂY

